Уравнение состояния идеального газа Менделеева-Клапейрона с выводом
Уравнение состояния идеального газа показывает корреляцию его основных макропараметров, а именно: объема V, давления P, а также температуры T.
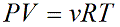
P – давление [Па]
V- объем [м3]
ν - количество вещества [моль]
R – универсальная газовая постоянная, 8,31 [Дж/(моль · К)]
T – температура [K]
Данную формулу также называют уравнением Менделеева-Клапейрона для идеального газа в честь двух ученых впервые получившего (Бенуа Клапейрон (1799 – 1864)) и применившего (Дмитрий Иванович Менделеев (1834 – 1907)) его.
Вывод уравнения Менделеева-Клапейрона
Давление идеального газа зависит от концентрации частиц и температуры тела:
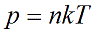
n - концентрация частиц [м-3]
k – константа Больцмана k = 1,38 · 10-23 [Дж/К]
Т – абсолютная температура, в кельвинах [К]
Возьмем основное уравнение МКТ, выведенное через кинетическую энергию:
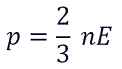
Подставим nkT вместо давления и выразим кинетическую энергию:
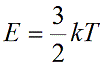
Концентрация частиц газа n равна:
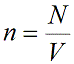
N – число молекул газа в емкости объемом V [м3]. N также можно представить как произведение количества вещества ν и числа Авогадро NA:
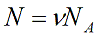
Подставим эти величины в уравнение давления идеального газа (p=nkT):
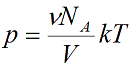
Произведение числа Авогадро NA и константы Больцмана k дает универсальную газовую постоянную R, которая равна 8,31 [Дж/(моль · К)]. Используя это, упростим уравнение давления и получим искомое уравнение состояния идеального газа:
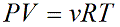
Учитывая, что количество вещества ν также можно определить, если известны масса вещества m и его молярная масса M:
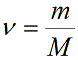
можно привести уравнение к следующему виду:
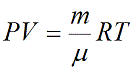
Частными случаями уравнения являются газовые законы, описывающие изопроцессы в идеальных газах, т.е. процессы, при которых один из макропараметров (T, P, V) в закрытой изолированной системе постоянный. Всего этих частных случаев 3.
Закон Бойля-Мариотта - изотермический процесс
Проходит при постоянной температуре: T= const.
P·V = const, то есть для конкретного вещества произведение давления на объем остается постоянным:
P1·V1 = P2·V2.
Закон Гей-Люссака - изобарный процесс
Проходит при постоянном давлении: P = const.
V/T = const, то есть для конкретного вещества отношение объема и температуры остается постоянным:
V1/T1 = V2/T2.
Закон Шарля - изобарный процесс
Проходит при постоянном объеме: V = const.
P/T = const, то есть для конкретного вещества отношение давления и температуры остается постоянным:
P1/T1 = P2/T2.
Скорее всего, Вам будет интересно:
- Основное уравнение молекулярно-кинетической теории (МКТ) с выводом
- Основные положения молекулярно-кинетической теории (МКТ), формулы МКТ
- Закон Кулона: формулировка, определение, формула
- Средняя линия трапеции: чему равна, свойства, доказательство теоремы
- Свойства вписанной в треугольник окружности
- Плотность тока проводимости, смещения, насыщения: определение и формулы
- Состав служебного программного обеспечения
- Свойства прямоугольной трапеции
- Как найти область определения функции онлайн
- Первый признак равенства треугольников: формулировка и доказательство (7 класс)
